Sociedad
Coronavirus
Bruselas autoriza el uso de la vacuna de Pfizer en la UE
AGENCIAS | EiTB MEDIA
La autorización llega horas después de que la Agencia Europea haya dado su visto a la vacuna. La distribución se realizará en los próximos días y las campañas de vacunación comenzarán el día 27.
-
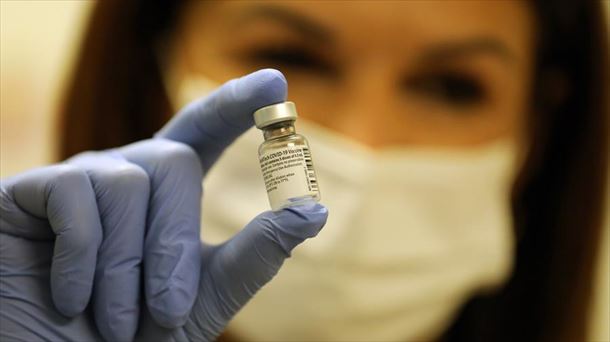
Una dosis de la vacuna de Pfizer. Foto de archivo: EFE
Euskaraz irakurri: Pfizerren txertoa merkaturatzeko baimena eman du Bruselak
La Comisión Europea (CE) ha otorgado una licencia condicional a Pfizer/BioNTech para el uso "al mismo tiempo y en las mismas condiciones" en los países europeos su vacuna contra la covid-19, lo que llega solo unas horas después de que la Agencia Europea del Medicamento (EMA) haya respaldado el fármaco.
En una breve comparecencia, la presidenta de la CE, Úrsula von der Leyen, ha asegurado que este lunes se ha abierto "un capítulo importante contra la pandemia" y ha explicado que otorgar la licencia condicional a la vacuna permitirá lanzar las campañas de vacunación el próximo día 27, teniendo en cuenta que las dosis se empezarán a repartir "en los próximos días" desde la fábrica de Pfizer en Bélgica.
"Durante esta pandemia, siempre he dicho que estamos juntos en esto. La vacunación puede comenzar al mismo tiempo, durante las jornadas de vacunación en la Unión Europea los días 27, 28 y 29 de diciembre. Esta es una buena manera de terminar este año tan difícil y finalmente empezar a pasar página en lo que respecta al covid-19", ha agregado Von der Leyen.
Asimismo, ha recordado que esta es la primera vacuna que se aprueba en territorio comunitario, pero "se aprobarán más si se demuestra que son seguras y eficaces", como la desarrollada por la farmacéutica Moderna, que los expertos en medicamentos humanos de la EMA prevén terminar de evaluar el próximo 6 de enero.
La presidenta de la CE, que ha prometido "ayudar a garantizar (este fármaco) para el resto del mundo, mientras se distribuyen las vacunas para los europeos", ha asegurado estar "orgullosa de que la primera vacuna del covid-19 disponible en Europa sea un verdadero producto de innovación europea".
La empresa BioNTech es alemana y recibió más de 9 millones de euros en la última década de los fondos de investigación de la UE, lo que le ha permitido desarrollar tecnologías realmente innovadoras que llevaron a la fabricación de esta vacuna contra el covid-19, algo que Von der Leyen ha resumido como "una verdadera historia de éxito de la Unión Europea".
Avalada por un ensayo de más de 43 000 personas
Previamente, la Agencia Europea del Medicamento ha dado su visto bueno a la vacuna contra la covid-19 desarrollada por Pfizer/BioNTech, el paso previo para que la Comisión Europea otorgue esta semana la licencia de uso condicional del fármaco en los países europeos.
"La evaluación científica de la EMA se basa en la fuerza de las pruebas científicas sobre la seguridad, calidad y eficacia de la vacuna, y nada más. Las pruebas demuestran de forma convincente que los beneficios son mayores que los riesgos de esta vacuna", ha señalado la directora ejecutiva de la EMA, Emer Cooke.
También ha defendido que este dictamen científico de la EMA garantiza que la vacuna llegará a Europa "con las correspondientes salvaguardias, controles y obligaciones".
"Nuestra evaluación exhaustiva significa que podemos asegurar con confianza a los ciudadanos de la UE la seguridad y eficacia de esta vacuna y que cumple las normas de calidad necesarias. Sin embargo, nuestro trabajo no se detiene aquí. Seguiremos recogiendo y analizando datos sobre la seguridad y la eficacia de esta vacuna para proteger a las personas que la toman en la UE", ha asegurado.
La presidenta del Comité de Seguridad de la EMA, Sabine Straus, ha defendido que "el perfil de seguridad de la vacuna de covid-19 a partir de los datos evaluados es tranquilizador". "La UE tiene un excelente sistema de vigilancia de la seguridad, con análisis y detección de última generación, para asegurar que identificamos la información de seguridad nueva o cambiante", ha añadido.
Por su parte, el presidente del CHMP, Harald Enzmann, ha resaltado que el principal ensayo clínico de esta vacuna, en el que participaron más de 43 000 personas, es "uno de los más grandes evaluados para una vacuna". La mitad recibió la vacuna y la otra mitad recibió una inyección falsa, es decir, placebo. Las personas no sabían si recibieron la vacuna o el placebo.
Se calculó la eficacia en más de 36 000 personas a partir de los 16 años de edad (incluidas las personas mayores de 75 años) que no tenían ningún signo de infección previa. El estudio mostró una reducción del 95 % en el número de casos sintomáticos de covid-19 en las personas que recibieron la vacuna (8 casos de 18 198 presentaron síntomas de covid-19) en comparación con las personas que recibieron una inyección ficticia (162 casos de 18 325 presentaron síntomas de covid-19).
El ensayo también demostró una eficacia de alrededor del 95 % en los participantes con riesgo de padecer covid-19 grave, incluidos aquellos con asma, enfermedad pulmonar crónica, diabetes, hipertensión arterial o un índice de masa corporal mayor a 30. La alta eficacia se mantuvo en todos los géneros, grupos raciales y étnicos.